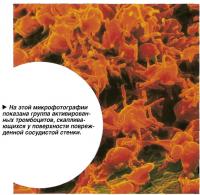
В обычных условиях кровь находится в сосудистом русле в жидком состоянии благодаря наличию в кровотоке естественных антикоагулянтов.
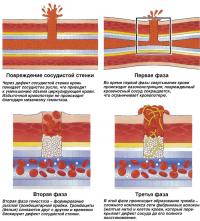
При повреждении сосудистой стенки запускается каскад химических реакций, направленных на остановку кровотечения, - гемостаз. При патологии гемостатических механизмов даже мелкая ранка может привести к смертельному кровотечению.
В процессе гемостаза участвуют многочисленные факторы коагуляции (свертывания крови), присутствующие в плазме, а также химические вещества, которые высвобождаются из тромбоцитов и поврежденных клеток.
Фазы гемостаза
Процесс гемостаза включает три основные фазы, быстро следующие друг за другом после повреждения сосуда.
Вазоконстрикция - первым элементом остановки кровотечения является сокращение поврежденного кровеносного сосуда; этот механизм может быстро и существенно снизить кровопотерю.
Формирование тромбоцитарной пробки - травматизация сосудистой стенки приводит к активации тромбоцитов, находящихся в плазме крови, которые слипаются друг с другом в месте дефекта сосудистой стенки с образованием рыхлой тромбоцитарной пробки.
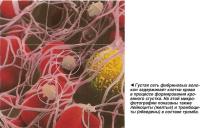
Коагуляция, образование кровяного сгустка - массу слипшихся тромбоцитов пронизывают нити фибрина. В сеть фибриновых волокон попадают эритроциты и лейкоциты, в результате чего формируется вторичная гемостатическая пробка - тромб.
Как формируется тромб
Формирование кровяного сгустка-чрезвычайно сложный процесс, требующий участия более 30 различных химических веществ. Некоторые из них -факторы коагуляции - стимулируют свертывание крови, другие - антикоагулянты - ингибируют (тормозят).
Процесс свертывания крови запускает каскад биохимических реакций, протекающих с участием тринадцати факторов коагуляции. Формируется сложный ферментативный комплекс - активатор протромбина, который способствует превращению плазменного белка протромбина в более мелкий белок - тромбин. Тромбин, в свою очередь, катализирует взаимодействие молекул фибриногена, находящихся в плазме крови, с образованием ячеистой структуры - сети фибриновых волокон. Эта сеть улавливает кровяные клетки, выходящие из кровотока через дефект в сосудистой стенке.
Огромное количество участников процесса гемостаза требует тщательной и точной регуляции. Нарушения регуляции процесса свертывания крови могут быть очень опасны: например, избыточное тромбообразование может привести к закупорке сосудов, кровоснабжающих те или иные органы или конечности.
Ретракция (сокращение) тромба и восстановление стенки сосуда
Через 30-60 минут после формирования тромба тромбоциты внутри него начинают сокращаться подобно мышце за счет входящих в их состав сократительных белков - актина и миозина. Это сокращение сопровождается натягиванием фибриновых нитей и соединением краев дефекта кровеносного сосуда и затягиванием ранки.
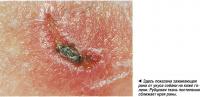
Кровяной сгусток - временное явление; во время сокращения тромба клетки окружающих тканей начинают делиться для закрытия дефекта сосудистой стенки.
Фибринолиз
После заживления ранки (примерно через два дня) сеть фибриновых волокон, составляющая основу тромба, рассасывается. Этот процесс, называемый фибринолизом, катализирует белок плазмин, который образуется из плазминогена.
Молекулы плазминогена с самого начала входят в состав кровяного сгустка, но их активация происходит только с началом процесса заживления. Б результате большая часть плазмина образуется прямо внутри тромба.
В норме в организме человека активность коагуляции и фибри-нолиза тонко сбалансирована.
Тромбоциты
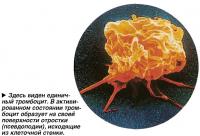
Тромбоциты (кровяные пластинки) в системе циркуляции имеют продолжительность жизни до 10 дней. Образуются в костном мозге из очень крупных клеток - мега-кариоцитов. Строго говоря, это не клетки в обычном понимании, поскольку они не имеют ядра и не способны к делению.
На электронной микрофотографии можно увидеть три составляющие тромбоцита.
- Наружная мембрана образована гликопротеиновой оболочкой, позволяющей тромбоциту прикрепляться только к поврежденным тканям. Мембрана содержит большое количество фосфолипидов, которые играют разнообразные роли в процессе свертывания крови.
- Цитозоль (раствор внутри клеточной мембраны) включает сократительные белки (актини миозин), микрофиламенты и микротубулы. Эти компоненты принимают участие в процессе ретракции кровяного сгустка.
- Тромбоцитарные гранулы содержат большое количество разнообразных гемостатически активных субстанций, которые высвобождаются при активации кровяных пластинок. Эти вещества способствуют агрегации (слипанию) тромбоцитов, привлекая их в место повреждения. Таким образом, формирование кровяного сгустка -процесс во многом саморегулирующийся.
Антикоагулянтные препараты
Основным клиническим назначением препаратов из группы антикоагулянтов является профилактика тромбообразования в неповрежденных сосудах. Крупный тромб может заблокировать кровеносный сосуд, что приведет к гибели кровоснабжаемых им тканей.
Клиническое применение
Антикоагулянты, такие как гепарин, вводятся парэнтерально (инъекционно), в то время как другие препараты, например варфарин, назначаются внутрь. Эти два лекарства имеют разный механизм действия; если эффект варфарина развивается в течение 48-72 часов, то гепарин действует моментально.
Гепарин является самым часто используемым лекарством из группы антикоагулянтов; его назначают при операциях на сердце и переливании крови. Варфарин применяется главным образом в качестве профилактического средства у пациентов, страдающих сердечной аритмией (нарушениями ритма сердца).
Ацетилсалициловая кислота блокирует агрегацию тромбоцитов и формирование тромбоци-тарной пробки. Как средство вторичной профилактики назначается пациентам, перенесшим ишемический инсульт или инфаркт миокарда.
Гемофилия
Гемофилия - это группа наслед-ственных заболеваний системы гемостаза, обусловленных недостатком одного из факторов свертывания крови. В большинстве случаев (до 85%) имеет место гемофилия А, причиной которой является дефицит фактора свертывания VIII. Заболевание характеризуется спонтанными кровоизлияниями в мышцы и суставы.
Для лечения заболевания применяют в числе прочего переливание человеческой плазмы в качестве источника недостающего фактора свертывания. В отношении пациентов, организм которых не вырабатывает факторы VIII или IX (болезнь Кристмаса), в настоящее время разрабатываются генно-инженерные методы лечения.
Тело человека. Снаружи и внутри. №45 2009